

- ΟΞΕΙΔΟΑΝΑΓΩΓΗ
- Εισαγωγή
- Αριθμός οξείδωσης
- Οξείδωση-Αναγωγή
- Οξειδωτικά-Αναγωγικά
- Ημιαντιδράσεις οξείδωσης-αναγωγής
- Αντιδράσεις οξειδοαναγωγής με τη μέθοδο ημιαντιδράσεων
- ΙΔΙΟΤΗΤΕΣ ΜΕΤΑΛΛΩΝ-ΑΓΩΓΟΙ
- Εισαγωγή
- Δομή μεταλλικού πλέγματος
- Δραστικότητα μετάλλων
- Ηλεκτροδιαλυτική τάση μετάλλων
- Ηλεκτρικοί αγωγοί
- ΓΑΛΒΑΝΙΚΑ ΣΤΟΙΧΕΙΑ
- Εισαγωγή
- Γαλβανικά στοιχεία
- Ημιστοιχεία-Ε ημιστοιχείων
- Ε0 ημιστοιχείων
- Γέφυρα άλατος
- Συμβολισμός ημιστοιχείου-Ηλεκτρόδια ημιστοιχείων
- Συμβολισμός γαλβανικού στοιχείου
- Ε στοιχείου - Ε0 στοιχείου-Υπολογισμοί Ε0
- Γραφή συνολικής αντίδρασης στοιχείου
- Παραδείγματα γραφής στοιχείων
- ΔG οξειδοαναγωγικής αντίδρασης
- Εξίσωση Nerst
- Παραδείγματα χρήσης εξίσωσης Nerst
- Εφαρμογές στοιχείων -Μπαταρίες
- ΠΕΙΡΑΜΑ - Στοιχείο Daniell
- ΗΛΕΚΤΡΟΛΥΣΗ
- Ηλεκτρολυτικά στοιχεία
- Προϊόντα ηλεκτρόλυσης
- Σύγκριση γαλβανικού – ηλεκτρολυτικού στοιχείου
- Παραδείγματα ηλεκτρόλυσης
- Νόμοι Faraday
- ΠΕΙΡΑΜΑ - Ηλεκτρόλυση Η2Ο ή αρ.δ. H2SO4
2.5 Ηλεκτρικοί αγωγοί
Τα διάφορα υλικά σώματα διακρίνονται σε αγωγούς και σε μονωτές ανάλογα με το αν είναι ή όχι δυνατή η κίνηση σε αυτά ηλεκτρικά φορτισμένων σωματιδίων.
Επομένως ένα σώμα χαρακτηρίζεται ως ηλεκτρικός αγωγός όταν υπάρχουν σ’ αυτό ηλεκτρικά φορτία και ακόμη όταν είναι δυνατή η κίνηση αυτών των φορτίων.
Στους ηλεκτρικούς αγωγούς ανήκουν:
A) Οι μεταλλικοί αγωγοί:
Όλα τα μέταλλα, τα κράματα και ορισμένα αμέταλλα όπως ο γραφίτης.
B) Οι ηλεκτρολυτικοί αγωγοί:
Τα τήγματα των αλάτων, καθώς και των υδροξειδίων και πολλών οξειδίων των μετάλλων.
Τα υδατικά διαλύματα των οξέων, των βάσεων και των αλάτων.
Όταν εφαρμόσουμε μία διαφορά δυναμικού μεταξύ δύο σημείων ενός ηλεκτρικού αγωγού, τότε τα ευκίνητα ηλεκτρικά φορτία του, αρχίζουν να κινούνται.
Στην περίπτωση ενός μεταλλικού αγωγού, η ηλεκτρική αγωγιμότητά του οφείλεται στην ύπαρξη των ελεύθερων ηλεκτρονίων του μεταλλικού πλέγματος. Έτσι εάν συνδέσουμε έναν μεταλλικό αγωγό με τους πόλους μιας πηγής (π.χ. μιας μπαταρίας), ισχύουν τα εξής:
-
Τα ηλεκτρικά φορτία, στην κίνηση των οποίων οφείλεται το ηλεκτρικό ρεύμα που διαρρέει τους μεταλλικούς αγωγούς, είναι τα ελεύθερα ηλεκτρόνια, τα οποία κινούνται όλα προς την ίδια κατεύθυνση.
- Τα θετικά ιόντα του μεταλλικού πλέγματος δε μετατοπίζονται.
-
Πραγματοποιείται συνεχής ροή ηλεκτρονίων από τον αρνητικό προς το θετικό πόλο της πηγής κατά μήκος του αγωγού. Στο εσωτερικό της ηλεκτρικής πηγής συνεχίζεται η ροή των ηλεκτρονίων από το θετικό προς τον αρνητικό πόλο της.
- Ο συνολικός αριθμός των ηλεκτρονίων στον αγωγό παραμένει συνεχώς σταθερός.
-
Το ηλεκτρικό ρεύμα (ηλεκτρόνια) που διαρρέει ένα μεταλλικό αγωγό, δεν προκαλεί καμία χημική αλλοίωση σ’ αυτόν.
Στην περίπτωση των ηλεκτρολυτικών αγωγών, η αγωγιμότητά τους οφείλεται στην ύπαρξη «ελεύθερων» ιόντων.
Συμπερασματικά:
Εάν συγκρίνουμε έναν μεταλλικό και έναν ηλεκτρολυτικό αγωγό μπορούμε να διακρίνουμε τις εξής διαφορές:
Διαφορές μεταλλικών και ηλεκτρολυτικών αγωγών:
1) Η αγωγιμότητα των μεταλλικών αγωγών οφείλεται στα ελεύθερα ηλεκτρόνια, ενώ των ηλεκτρολυτικών αγωγών στα «ελεύθερα» ιόντα.
2) Τα αποτελέσματα της διέλευσης του ηλεκτρικού ρεύματος μέσα από τους μεταλλικούς αγωγούς είναι κυρίως θερμικά (δε μεταβάλλεται η χημική τους σύσταση), ενώ μέσα από ηλεκτρολυτικούς αγωγούς είναι κυρίως χημικά.
3) Με την αύξηση της θερμοκρασίας η αγωγιμότητα των μεταλλικών αγωγών ελαττώνεται ενώ των ηλεκτρολυτικών αυξάνεται.
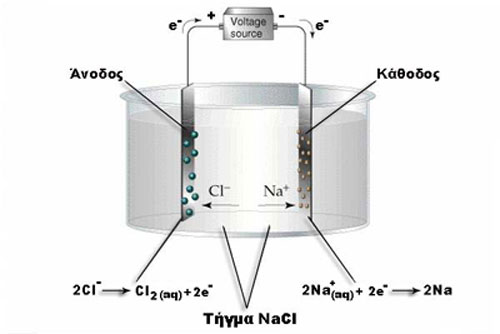
Ηλεκτρόλυση τήγματος NaCl
Διακρίνεται η μετακίνηση e- στο εξωτερικό κύκλωμα μέσω μεταλλικού αγωγού (μεταλλικός αγωγός) και η μετακίνηση ιόντων, Νa+ και Cl-, μέσα στο τήγμα του ηλεκτρολύτη (ηλεκτρολυτικός αγωγός).
|